Sauerstoff (O) ist das häufigste Element in der Erdhülle (bis 16 km Tiefe) und der Erdkruste (bis 35 km Tiefe). Dort befindet es sich allerdings nicht als zweiatomiges, gasförmiges O2 wie in der Luft, sondern in Verbindung mit anderen Elementen.
Oxide
Wenn Sauerstoff nur mit einem anderen Element verbunden ist, spricht man von Oxiden (Tabelle 1).
Tabelle 1: Liste der Oxide
| Verbundenes Element | Sauerstoffverbindung | Trivialname |
| Wasserstoff (H) | Wasserstoffoxid, H2O | Wasser |
| Aluminium (Al) | Aluminiumoxid, Al2O3 | Tonerde |
| Eisen (Fe) | Eisenoxid, Fe2O3 | Rost |
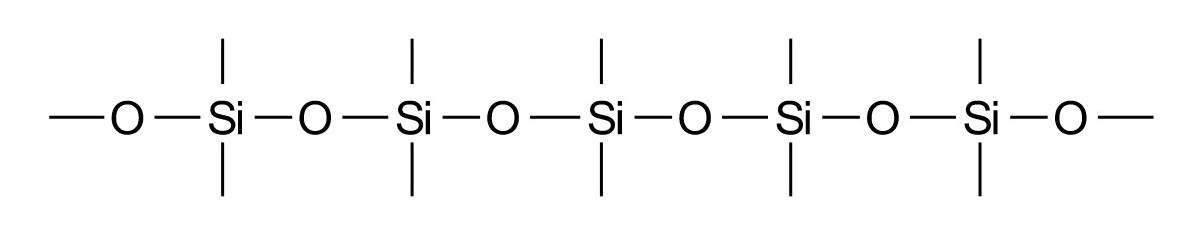
| Silizium (Si) | Siliziumdioxid, SiO2 | (Quarz-)Sand |
| Stickstoff (N) | Stickstoffdioxid, NO2 | Stickoxid |
| Kohlenstoff (C) | Kohlenstoffdioxid, CO2 | Kohlendioxid |
| Schwefel (S) | Schwefeldioxid, SO2 | Schwefeldioxid |
| Magnesium (Mg) | Magnesiumoxid, MgO | Magnesia |
Wenn noch weitere Elemente beteiligt sind, hat man es häufig mit Stoffen zu tun, die mitunter ganze Gebirge bilden (Tabelle 2).
Tabelle 2: Sauerstoffverbindungen mit weiteren Elementen
| Verbundene Elemente | Sauerstoffverbindung | Trivialname |
| Calcium (Ca), Kohlenstoff (C) | Calciumcarbonat, CaCO3 | Kalkstein, Kreide, Marmor |
| Calcium (Ca), Magnesium (Mg), Kohlenstoff (C) | Calciummagnesiumcarbonat, CaMg(CO3)2 | Dolomit |
| Calcium (Ca), Schwefel (S) | Calciumsulfat, CaSO4 | Gips, Anhydrid |
| Aluminium (Al), Silizium (Si) | Aluminiumsilikat, Al2(SiO3)3 | Ton |
Weitere Sauerstoffverbindungen
Während Wasser als flüssiges Oxid der häufigste Kosmetik-Inhaltsstoff sein dürfte, finden sich unter den festen Oxiden viele Pigmente im dekorativen Bereich – z. B. Eisenoxide (rot, braun, schwarz) und Titandioxid (weiß). Calciumsulfat ist in erhärtenden Masken und Modelagen zu finden. Sand, Ton und Eisenoxide sind die Hauptbestandteile von Lehm und Heilerden, die als (Reinigungs-)Masken dienen können oder in der Physiotherapie zum Einsatz kommen.
Essigsaure Tonerde ist trotz Aluminiumdiskussion ein weit verbreitetes adstringierendes Mittel in der Medizin. Allerdings ist der Name etwas irreführend, da Tonerde wie oben angegeben darin nicht mehr existent ist, sondern es sich um Salze des Aluminiums handelt, die sich bei der Reaktion von Tonerde mit Essigsäure (Acetate) oder Weinsäure (Tartrate) bilden.
Beides sind organische Carbonsäuren, die Sauerstoff neben Kohlenstoff und Wasserstoff enthalten. Diese Carbonsäuren gehören zu einer außerordentlich großen Vielfalt von organischen Sauerstoffverbindungen. Die wichtigsten sind:
- Alkohole, wie z. B. Ethanol (Trinkalkohol), Isopropanol (häufige Alternative als Desinfektionsmittel), Benzylalkohol (Konservierungsstoff) und Glycerin (Teil des körpereigenen NMF),
- Aldehyde und Ketone, zu denen viele Riechstoffe wie das Citronellal (Limette) und das Muscon (Moschus) gehören,
- Carbonsäuren wie Essigsäure, Zitronensäure, Salicylsäure und essenzielle Fettsäuren (Linolsäure, α-Linolensäure etc.) sowie ihre
- Verbindungen untereinander – wie z. B. Ether („Äther“ aus 2 x Ethanol) oder Ester (aus Alkohol und Carbonsäure). Hauptbestandteil der Pflanzenöle und tierischer Fette sind Triglyceride; das sind Ester aus Glycerin und drei Carbonsäuren.
Alkohole, Carbonsäuren und Carbonsäureester sind in Kosmetika häufig anzutreffen und übernehmen dort beispielsweise Funktionen als Lösungsmittel, Spreiter, Säurepeeling, Konsistenzgeber, fettende Komponenten und Wirkstoffe.
Die Zahl der Sauerstoffverbindungen in lebenden Organismen steigt weiter, wenn noch das Element Stickstoff, etwa in Aminosäuren, Peptiden und Proteinen, oder andere Elemente wie Phosphor und Spurenelemente hinzukommen.
Sauerstofffreie Verbindungen wie Kohlenwasserstoffe – ein Beispiel ist das im menschlichen Sebum vorkommende Squalen – sind eher die Ausnahme oder kommen im Zusammenhang mit anaeroben, also unter Sauerstoffausschluss lebenden Mikroorganismen vor. Beispiel: Methanbildung in den Mägen von Wiederkäuern.
Oxidation
Sauerstoff ist ein sehr reaktionsfähiges Element, das jedoch zum Glück eine gewisse Aktivierungsenergie (hohe Temperatur, Streichholz, Strahlung) benötigt, um sich mit brennbaren, sprich oxidierbaren Stoffen in einer sich beschleunigenden Kettenreaktion umzusetzen. Ohne diese Schwelle wäre eine Welt, wie wir sie kennen, nicht möglich, da nahezu alles sofort verbrennen bzw. oxidiert werden würde.
Bei Oxidationen entsteht Energie, die nicht nur in Kraftwerken zur Elektrizitätserzeugung und in Autos zur Fortbewegung genutzt, sondern auch in unserem Körper zur Aufrechterhaltung der Körpertemperatur und zur Bereitstellung mechanischer Energie in den Muskeln erzeugt wird. Zu diesem Zweck gibt es in den menschlichen Zellen spezielle Organellen – die Mitochondrien. Die wichtigsten, dort ablaufenden Oxidationen sind:
- Abbau von Acetyl-Coenzym A im Zitronensäurezyklus,
- Abbau von Fettsäuren durch ß-Oxidation und
- Oxidation von Glucose (Traubenzucker).
Analog einer Brennstoffzelle laufen die Oxidationen dort biochemisch kontrolliert ab. Die einzelnen Reaktionsschritte werden durch Enzyme (Oxidoreduktasen) katalysiert, d. h. mit geringstmöglicher Aktivierungsenergie durchgeführt. Dabei finden unter anderem auch radikalische Reaktionen statt. Endprodukte sind Kohlendioxid, das ausgeatmet wird, sowie Wasser und oxidierte organische Verbindungen, die hauptsächlich über Kot und Urin ausgeschieden werden. Der im Urin enthaltene Harnstoff koppelt das Kohlendioxid an das Abfallprodukt Ammoniak.
Außerhalb der Mitochondrien können unkontrollierte radikalische Oxidationen Schäden anrichten. Deswegen werden die Zellen der Organismen durch Antioxidantien wie Vitamin C (Ascorbinsäure) und Vitamin E (Tocopherol) geschützt. In der Hautbarriere sind es dann die Aminosäuren des Natural Moisturizing Factor (NMF) und diverse Peptidstrukturen, die insbesondere gegen oxidierende atmosphärische Radikale wie Stickstoffoxide wirksam sind.
In der „freien“ Natur entstehen durch die gleichzeitige Einwirkung von Sauerstoff und energiereicher (UV-)Strahlung viele Schadstoffe. Beispiele sind:
- die photochemische Oxidation von pflanzlichen oder anthropogenen Kohlenwasserstoffen unter anderem zu Peroxyacetylnitrat (PAN), einem Bestandteil des atmosphärischen Smogs
- die Einwirkung von Ozon, das aus 3 Sauerstoffatomen (O3) besteht, auf organische Verbindungen
- die Bildung allergener Peroxide aus ätherischen Ölen, z. B. Ascaridol aus Teebaumöl
- die Peroxidierung ungesättigter Säuren. Dabei entstehen in der Folge Spaltprodukte (Aldehyde), die den ranzigen Geruch von Ölen und Fetten verursachen.
ROS und freie Radikale
Besonders aggressiv sind neben dem Ozon (O3) und dem energiereichen Singulettsauerstoff (1O2) das Peroxidanion (O22-), das Hydroxylradikal (HO•) und das Hyperoxidanion alias Superoxidanion (O2–). Sie gehören zur Gruppe der ROS (Reactive Oxygen Species). Die aus der unkontrollierten Reaktion mit organischen Verbindungen resultierenden organischen Hydroperoxide (R-OOH), Peroxyradikale (R-OO•) und Alkoxyradikale (R-O•) sind ebenfalls äußerst reaktiv und schädlich. Um ihre Bildung zu verhindern und sich dagegen zu schützen, werden in Lebensmitteln, Kosmetika und vielen anderen Gegenständen des täglichen Lebens Antioxidantien eingesetzt. Ihr Prinzip ist es, schneller mit ROS zu reagieren als die zu schützenden Zusammensetzungen. Dabei werden sie allerdings auch verbraucht. In Sonnenschutzmitteln geht man einen anderen Weg. Hier wird die Strahlung bereits mithilfe von UV-Filtern in Wärme umgewandelt, bevor sich Radikale bilden können.
Oxidative Wirkung auf die Haut
Schäden an Lipiden („Lipidperoxidation“) oder Proteinen („Proteinoxidation“) in der Haut initiieren Entzündungs- und Alterungsprozesse, DNA-Schäden sowie Hautveränderungen bis hin zu Karzinomen. Äußerlich erkennbar sind Altersflecken, die aus oxidierten Protein-Lipid-Komplexen (Lipofuszin) oder Zucker-Protein-Agglomeraten (Advanced Glycation Endproducts [AGE]) bestehen. Bei AGE reagieren Kohlenhydrate mit Aminosäuren und Proteinen und bilden in einem von Oxidation begleiteten Prozess sogenannte Melanoidine.
Im normalen physiologischen Stoffwechsel und bei Immunantworten bedient sich selbst der Körper der aggressiven ROS-Moleküle. Ein Beispiel ist Wasserstoffperoxid (H2O2), das Enzym-kontrolliert für spezielle biochemische Reaktionen benötigt wird. Überschüssiges Wasserstoffperoxid wird durch das Enzym Katalase (CAT) zu Wasser und Sauerstoff und durch die selenhaltige Glutathionperoxidase (GPX) zu Wasser abgebaut. So kann es im Organismus keine Schäden anrichten – es sei denn, es liegen Enzymdefekte vor.
Die sichtbare Folge eines Enzymdefektes ist zum Beispiel die Vitiligo (Weißfleckenkrankheit). In diesem Fall greift nicht abgebautes Wasserstoffperoxid Melanin und den Melanin-Bildungsprozess an. Die Haut bleibt unpigmentiert. Eine ähnliche Wirkung kann man beim Bleichen von Haut und Haaren mit Wasserstoffperoxid beobachten.
Auch die Hautflora bedient sich eigener Enzyme, die Lipide oxidieren und abbauen können. Dabei entstehen unter anderem kurzkettige Carbonsäuren, die den schützenden Säuremantel der Haut bilden und den pH senken.
Sauerstoff in der Therapie
Die Sauerstoff-Mehrschritt-Therapie1, die von M. von Ardenne entwickelt wurde, besteht in der Inhalation von reinem Sauerstoff oder der Erhöhung des Sauerstoffanteils in der Atemluft, nachdem oral ein Vitamin-Mix verabreicht wurde, gefolgt von einem geistig-körperlichen Training. Die dabei erhöhte Verfügbarkeit von Sauerstoff in den Arterien soll Heilungsprozesse bei diversen Indikationen beschleunigen. Statistisch gesicherte Wirkungsnachweise gibt es zu dieser Therapie jedoch nicht.
Reaktive Sauerstoffverbindungen wirken bei oberflächlichen Infekten und Mykosen aseptisch. Beispiele sind Benzoylperoxid zur Behandlung der Akne und ozonisierte Pflanzenöle.
Zur Flächendesinfektion von Gegenständen werden niedrigkonzentrierte Wasserstoffperoxid-Lösungen verwendet. Sie sind auch gut wirksam bei der Bekämpfung von Schimmel. Dabei wird hochreaktiver, naszierender (einatomiger) Sauerstoff freigesetzt. Häufig verwendete sauerstoffabgebende Verbindungen sind auch Kaliumpermanganat, das als schnell wirkendes Mittel bei Pilzinfekten und anderen Hautinfekten verwendet wird, sowie alkalische Hypochlorit-Lösungen (oxidative Reiniger).
Kosmetische Hochfrequenzstäbe erzeugen geringe Mengen an Ozon und Stickoxiden, die bei der Ausreinigung von Akne-Komedonen oder der Behandlung entzündeter Hautareale desinfizierend wirken. In kosmetischen Bedampfungsgeräten (Vapozon) entsteht Ozon an einer UV-Licht abstrahlenden Quarzlampe.
Was sonst noch interessant ist
Intramolekulare Oxidationen sind das Prinzip von Sprengstoffen. Die verheerende Explosion im August 2020 im Hafen von Beirut wurde durch die Zündung des salzähnlichen Ammoniumnitrats (NH4NO3) verursacht. Dabei oxidiert der sauerstoffreiche Nitrat-Teil (NO3–) in einer Blitzreaktion die Ammonium-Gruppe (NH4+) unter Bildung von gasförmigem Wasser (H2O), Stickstoff (N2), und Sauerstoff (O2).
Da eine Oxidation physikalisch immer mit einem Elektronenübergang von dem zu oxidierenden Stoff auf den Sauerstoff verbunden ist, spricht man generell auch dann von einer Oxidation, wenn einem Stoff in irgendeiner Weise Elektronen entzogen werden. Beispiel: Silber läuft bei der Reaktion mit Schwefelverbindungen schwarz an; dabei wird das elementare Silber (Ag) „oxidiert“, gibt ein Elektron ab und wird in eine ionische Silberverbindung (Ag+) umgewandelt.
Bei der Photosynthese der Pflanzen, die aus Wasser Sauerstoff produzieren, findet eine Oxidation des im Wasser enthaltenen Sauerstoffs (O2-) zu gasförmigem Sauerstoff (O2) statt, indem Elektronen abgegeben werden.
1) Wolfgang Schnizer, Birgit Siebert, Jürgen Kleinschmidt und Reinhard Erdl, Deutsches Ärzteblatt 1985 (82), 27: 2026-2030
Dr. Hans Lautenschläger